Plantas precisam de nitrogênio. E você está mergulhado nisso – o ar é 78% nitrogênio. O problema é, o tipo de nitrogênio que as plantas precisam é reduzido (isto é, tem mais elétrons) se comparado ao N2 que existe no ar. No passado, isso significava fazer rotação de culturas – amendoins, por exemplo, promovem a redução (química) do nitrogênio, ou bactéria “fixadora de nitrogênio”.
Aprendemos a algum tempo que poderíamos fixar o nosso próprio nitrogênio. O processo Haber-Bosch pode pegar nitrogênio (molécula) e hidrogênio (molécula) e produzir uma significativa quantidade de amônia – um nitrogênio reduzido ou “fixado”. Você pode usar amônia como fertilizante – se a manter em grandes tanques iguais a botijões de gás, também pode manter por aí a amônia líquida (que ferve abaixo de zero). Se misturar amônia com ácido nítrico, você pode fazer nitrato de amônio, um sólido fácil de manejar:
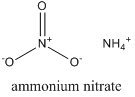
O problema é, o nitrato é um oxidante bem bom, e tem todo aquele nitrogênio reduzido em volta para reagir. O nitrato de amônio é na verdade um bom explosivo, e é ainda melhor se tiver algum combustível por perto – como o diesel. O combustível/nitrato de amônio, ou ANFO, foi usado pelo terrorista americano Timothy McVeigh no seu ataque ao prédio federal na cidade de Oklahoma (Estados Unidos).
O fato de um fertilizante, que é bastante comum, ter um componente com tal potencial explosivo, é objeto de muita preocupação. “Amanhã”*, uma solução para isso.
OBS*: Este texto foi originalmente escrito no blog “Molecule of the day”.
Original (English) content from Molecule of the Day (http://scienceblogs.com/moleculeoftheday). Content translated with permission, but portuguese text not reviewed by the original author. Please do not distribute beyond this site without permission from both author and translator.